
点击右上角![]() 微信好友
微信好友
 朋友圈
朋友圈

请使用浏览器分享功能进行分享

近两年,中国科兴在国家全方位的支持下,创造了令人瞩目的疫苗速度:2020年1月28日公司立项,76天获得临床批件,153天获批紧急使用,99天完成一期厂房建设,169天获得生产许可证,374天获得附条件上市批件,1年时间完成超20亿剂年产能构建,实现全球供应超27亿剂……

中国政府援助柬埔寨的科兴新冠疫苗。图自新华社
与病毒赛跑 疫苗三个月上临床
“接种疫苗是防控传染病最经济最有效的手段,没有疫苗就要去做疫苗,这是疫情防控的基本逻辑。”公司董事长、总裁兼CEO尹卫东表示,面对当时刚刚出现的新冠疫情,他立即下定决心:启动新冠疫苗的研究,并确保2020年4月拿出疫苗上临床。
获得病毒是新冠灭活疫苗研发的关键和前提,而想要病毒来源就必须要有P3实验室,这成了摆在科兴疫苗研发工作面前的第一道难题。
为了实现在紧急状态下快速组织动员全国优势力量实现特定科技创新的目标,国务院联防联控机制专门成立了疫苗研发专班,由卫生健康委、科技部、药品监督管理局等部门组成,有效联动政府部门、医疗卫生机构、科研院所、企业等多方力量,旨在尊重疫苗研发规律的前提下,最大限度地加快实现毒株分离、疫苗制备、动物试验、临床研究等工作。
2020年1月28日,中国科兴“克冠行动”正式立项,全面启动新冠灭活疫苗研制项目;1月30日,中国科兴首支科研团队进驻浙江省疾控中心P3实验室;2月23日,证明病毒灭活纯化后可激发动物产生中和抗体;3月3日,开始动物有效性试验;3月底,开始进行动物攻毒保护试验;4月13日,获批进入临床研究;5月6日,在《科学》杂志发布全球首个新冠疫苗能够让恒河猴抵御新冠病毒的科学结果……
新冠疫苗研发的目的不仅仅是做科学研究,更重要的是要控制疫情。如果像以往疫苗研发的路径那样先研发、再等待审批、再生产,明显赶不上疫情防控的需求。
在药审中心《抗新型冠状病毒药物特别审评工作方案》的“研审联动”工作机制推动下,新冠疫苗的研究与注册程序得以同步推进,从过去的“串联”改“并联”,并确保程序不减少、标准不降低甚至比过去更高。
在2020年3月16日至4月20日的34天内,单纯围绕新冠疫苗临床研究申请,科兴就经历了18轮预评审,注册检验7次,共完成7次抽样,共计完成10批原液及17批成品的抽样检验。平均每2天抽样一次检测一次。
2020年4月16日,科兴新型冠状病毒灭活疫苗克尔来福Ⅰ期临床研究正式启动。
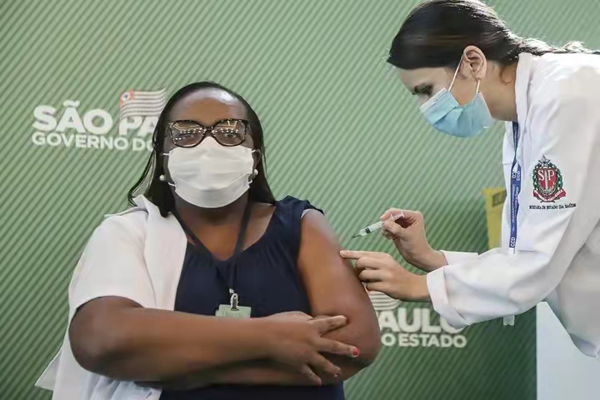
巴西首名新冠疫苗接种者莫妮卡·卡拉桑斯在圣保罗大学临床医院接种中国新冠疫苗克尔来福。图自新华社
产学研结合 “中国方案”展现协同优势
随着Ⅰ/Ⅱ期临床试验顺利完成,疫苗研发工作又遭遇了新的困难——Ⅲ期临床研究志愿者从哪来?
根据当时国家卫健委公布的数据,截至2020年4月8日,全国有累计确诊病例1160例,而且发现一例就收治一例,不存在疾病自然流行状态。而Ⅲ期临床需要在疾病流行状况下招募数以万计的志愿者。
若在境外开展大规模Ⅲ期临床研究,按照每位受试者数万元的费用,三个中心的临床试验则至少需近10亿元,而当时中国科兴旗下负责新冠疫苗研制的团队科兴中维总资产规模仅5000万元。
“以疫苗换临床!”尹卫东解释道,“也就是说我把疫苗给合作伙伴,他们来做临床,最后如果成功了,公司将优先并以明显低于市场水平的价格向他们提供疫苗,实现风险补偿。”
针对如何选择Ⅲ期临床合作国家,尹卫东提出了四条原则:一要人口众多,二要疫情严重,三没有疫苗研发或生产能力,四是该国具备较好的疫苗审评审批能力。根据以上原则,科兴公司将目光投向了巴西、印尼、土耳其和智利,并于2020年7月开始陆续开启海外临床研究。
尹卫东坦言,海外多个国家临床研究的顺利推进,得益于各国政府与中国的密切交流与合作,快速推动了中国与各方的科学理解与合作,极大推进了各国与国内科学结果的互认。“这是企业和个人难以企及和实现的效果,这不仅是一种全新的商业合作模式,更是科学研究上的战略合作。而且这些国家对周边地区具有极大带动性,迅速拓展了中国疫苗在南美地区和东南亚地区的合作。”

马来西亚吉隆坡郊区的发马公司灌装工厂,一名工人在包装本地灌装生产的科兴疫苗。图自新华社
与此同时,科兴也在国内开始了新冠疫苗的产业化布局。“想要通过疫苗来控制疫情,那就必须要让人人都能接种疫苗,14亿中国一人一剂,就是14亿剂,一人两剂,就是28亿剂,更何况,新冠疫苗这一仗不仅是为中国人民打的,而是为全世界而打。”尹卫东说。
为了实现每年20-30亿支的产能,保证国内新冠防控对疫苗的需要及对外供应,科兴公司陆续投入40多亿元建设新冠疫苗生产线和异地委托生产线。
“没有订单,不知道究竟需要多少疫苗,但科兴做出了每年20亿剂产能的决定。我们知道这个产能在未来疫情常态化以后绝对是过剩的,但现在国家需要,就必须做。产能过剩这个风险我可以量化,但国家需要疫苗却没有,这个风险是无法量化的。关键时刻,就是要有企业通过创新和勇于投入,去弥补短期不确定性下可能存在的风险。”尹卫东说。
2021年2月5日,国家药监局批准科兴新型冠状病毒灭活疫苗“克尔来福”在国内附条件上市。2021年6月1日世卫组织将中国科兴新冠疫苗列入“紧急使用清单”。此外,科兴新冠疫苗还获得了包括中国在内58个国家、组织、地区的准入许可。
2021年7月16日,中国工业和信息化部总工程师、新闻发言人田玉龙介绍中国疫苗生产供应情况时说,截至7月份,中国的新冠疫苗年生产产能达到了50亿剂,有效地保障了国内接种需求。
截至2022年1月29日,中国科兴的新冠疫苗全球出货量达27亿剂,单日最大发货量3722万剂,覆盖了全球52个国家和地区的20.52亿人口。
“新冠疫苗是以企业为主体、产学研相结合的疫苗研发和产业化体系协同而生的中国方案的一个典型案例。”尹卫东在接受采访时说。
全球更可及 新冠疫苗为全世界而研发
回顾两年以来的工作,尹卫东称,“累是真累,但在科研和产业化方面的收获也是巨大的。”
2月15日,两篇关于中国疫苗的最新重磅论文在《细胞》子刊和《柳叶刀》预印本网站上同日刊出,论文中基于科学研究的数据表明,中国疫苗对阻断新冠大流行已经起到了重要作用,并将持续对应对病毒变异发挥应有作用。
在尹卫东看来,未来,新冠疫情将趋于常态化,新冠疫苗的接种也将趋于常态化。“新冠疫情让我们意识到,今后中国应该与更多国家在传染病防控上谋求更多合作。”
2月23日,厄瓜多尔卫生部与中国科兴签订合作意向书,双方同意在厄建设一所生产新冠疫苗以及其他疫苗的工厂。
在过去的一年多时间里,中国科兴陆续帮助非洲、亚洲、拉美州等多个国家的合作伙伴实现了新冠疫苗的本地化生产,通过国际合作,真正做到让新冠疫苗在全球更可及。

科兴新冠疫苗埃及工厂,图自新华社。
受国家科技部委托,科兴中维承担了金砖国家疫苗研发中国中心建设工作。该中心将通过线上线下相结合的方式,推进五国疫苗联合研发和试验、合作建厂、授权生产、标准互认等工作。
下一步,该中心将联合金砖国家及更多国家,与各国高校、科研机构、卫生疾控机构和产业界合作,监测疾病流行变化与病毒变异、推动疫苗研究与产业化、探讨疫苗应用策略等,资助相关机构开展新冠疫苗的研究,面向全球优秀科学家发出邀请加入研究团队。
尹卫东说,“传染病这个问题一旦出现就不是一个国家、一个地区的问题,而是全世界的问题。中国企业赴海外投资建厂,同时还承担着与相关国家的政府机构与科研机构保持密切合作的职责,第一时间了解、获取这些国家的疾病和疫情的情况,并共同合作研发相关疫苗,在支援他们的同时,也实现保护我们自己的目标。”(赵清建)
