
点击右上角![]() 微信好友
微信好友
 朋友圈
朋友圈

请使用浏览器分享功能进行分享

近年来,随着生物科学技术的不断迭代演进,抗癌创新药在挽救患者生命的同时,也在掏空普通老百姓一辈子的积蓄,前有“我不是药神”,后有120万一针“天价抗癌药”,“创新药”与“低价”似乎成了一对反义词。
首药控股成立于2016年,是一家处于临床研究阶段的小分子创新药企业,在研管线多达23个,其中17个进入临床研究阶段,涵盖了非小细胞肺癌、淋巴瘤、肝细胞癌、胰腺癌、甲状腺癌、卵巢癌、白血病等重点肿瘤适应症以及Ⅱ型糖尿病等其他重要疾病领域。
首药控股是一家强调社会责任感的创新药公司,他们的目标是通过科研工作者的努力,创好药,提高肿瘤患者的生存周期和生存质量,能够让多种肿瘤患者长期带瘤生存,最终实现“把肿瘤当成慢性病,甚至感冒来治”。这看似遥不可及的目标,首药控股正在通过它的方式努力实践着。
近日,首药控股即将在科创板上市,拟募集资金20亿元,用于创新药研发项目、新药研发与产业化基地以及补充流动资金。
23个研发管线,研发能力出众
近年来,大量biotech生物公司仅凭一两条重磅研发管线就能登上港股或A股科创板,对于一个尚未有产品上市的创新药企而言,研发管线的差异性及丰富程度是衡量企业前景的重要因素。
目前,首药控股在全球范围内获得140项发明专利,研发管线共有23个在研项目,均为1类新药,其中11个为完全自主研发,12个为合作研发。
进入临床研究是创新药研发的重要里程碑,首药控股研发管线中有17个已进入临床研究阶段,在同等体量的创新药企中,处于领先水平。
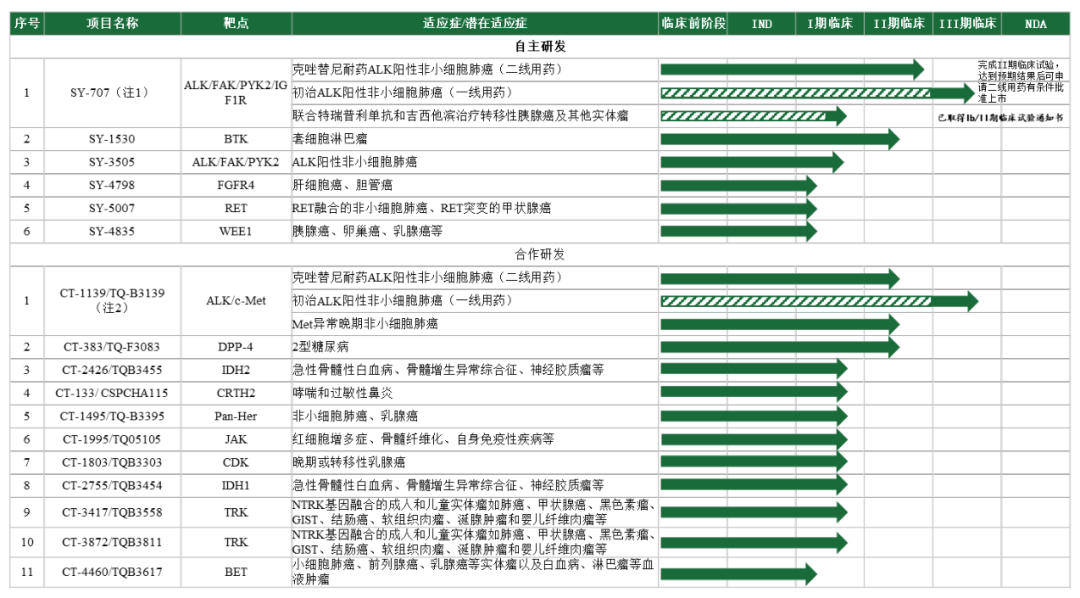
处于临床阶段的候选药物管线
来源:招股书
其中自主研发管线有1个在研产品已进入Ⅱ/Ⅲ 期临床试验,1个在研产品进入Ⅱ期临床试验,4个在研产品进入Ⅰ期临床试验,研发管线靶点丰富、梯次分明、不乏差异性:
◆SY-707
第二代ALK激酶多靶点抑制剂,用于治疗晚期ALK阳性非小细胞肺癌患者。目前正在同步开展针对克唑替尼耐药的ALK阳性非小细胞肺癌患者二线用药的II期临床试验以及针对初治ALK阳性非小细胞肺癌患者一线用药的III期临床试验。
同时,CDE同意SY-707在完成 II期临床试验,达到预期结果后可申请有条件批准上市(二线用药)。鉴于 SY-707 为 ALK/FAK/PYK2/IGF1R 多靶点抑制剂,首药控股正积极探索SY-707其他潜在适应症,2021年10月,SY-707 联合特瑞普利单抗和吉西他滨治疗转移性胰腺癌及其他实体瘤的临床试验申请已获得国家药监局通过。
◆SY-3505
第三代ALK抑制剂,是国内第一个进行临床试验的国产三代 ALK 抑制剂,主要用于治疗一、二代 ALK抑制剂耐药的ALK阳性非小细胞肺癌。
目前全球仅有一款三代 ALK 抑制剂劳拉替尼获批但尚未在中国大陆地区上市,SY-3505 作为国内首个进入临床研究的国产三代 ALK 抑制剂,已在临床Ⅰ期研究的耐药患者中初见疗效,其研发进度在国内临床研究中处于前沿水平。
◆SY-1530
二代高选择性 BTK 抑制剂,主要用于治疗多种B细胞来源的血液肿瘤(包括多种类型的非霍奇金淋巴瘤)。
目前已完成 I 期临床试验,产品已显示出良好的安全性以及对多种非霍奇金淋巴瘤的显著治疗效果,目前正在开展针对复发或难治套细胞淋巴瘤适应症的Ⅱ期临床试验。
◆SY-5007
选择性RET抑制剂,正在进行的Ⅰ期临床试验包括剂量爬坡和剂量拓展阶段,适应症涵盖RET基因变异的非小细胞肺癌、甲状腺癌等实体肿瘤。
目前,全球范围仅有两个选择性RET抑制剂获批,其中一款在国内获批上市,SY-5007是中国首个进入临床阶段的国产自主研发选择性RET抑制剂,研发进度领先。
◆SY-4835
正在进行Ⅰ期临床的WEE1抑制剂,其潜在适应症包括胰腺癌、卵巢癌、乳腺癌等多种实体瘤和AML等血液肿瘤。
全球范围内尚无 WEE1抑制剂获批上市,SY-4835 是临床试验进度处于第一梯队的国产WEE1抑制剂药物。
◆SY-4798
高选择性、高活性FGFR4抑制剂,目前正在进行Ⅰ期临床研究,其潜在适应症包括肝细胞癌在内的多种消化系统肿瘤。
目前高选择性FGFR4抑制剂在国内外均未有药物上市,几个候选品种均处于临床研究阶段。相比于泛FGFR抑制剂,高选择性 FGFR4抑制剂可以显著减少由于脱靶效应而导致的不良事件。
除了自主研发项目,首药控股在临床前药物研发创新能力也获得了同行的认可,正大天晴、石药中奇等知名药企主动寻求合作,首药控股主要负责临床前候选药物的发现及筛选,在完成小试合成工艺交接后,与正大天晴或石药中奇等合作进行后续的 GLP 毒理实验、临床研发及商业化。
合作研发模式下,首药控股与对方共同拥有合同项下的专利权、著作权等知识产权,首药控股按协议约定享有里程碑付款和商业化权益。
高达23个研发管线让首药控股在一众创新药企中脱颖而出,虽然部分管线存在同质化竞争,但对于患者而言,更多的竞争,带来的是更多的选择,以及更低的价格。
造中国患者能够吃得起的一类新药
一款创新药的诞生,背后是往往是巨额的资金投入以及大量时间付出,而付出所获得的回报也是诱人的,贝达药业仅凭一款凯美纳十年销售额就超100亿元。
药企不遗余力的投入研发,为的是在创新药专利到期前获得超额的利润,因此专利到期前的产品售价往往也是远超成本的。然而,对于中低收入患者而言,为了挽回健康甚至是生命,不得不付出自身无法承受的代价,这也让创新药陷入了伦理困境。
然而,首药控股却敢于直面挑战,试图挑战创新药的伦理困境。打开首药控股官网的首页,映入眼帘的便是两行大字——“造中国患者能够吃得起的一类新药”。
这两行字看似是首药控股在自我标榜,或是立了一个遥不可及的目标,但首药控股却实实在在地正朝着这个方向稳步前进。
首先是研发效率上,首药控股利用自有核心技术,通过以交替穿插、多线并行的研发模式替代传统单线循环的研究路径,在化合物分子设计及结构优化阶段兼顾化合物的靶点选择性、结合力以及化合物的药代动力学性质,降低新药研发中靶点失败的风险,运用计算机辅助药物设计及先导化合物优化技术开展药物分子设计及结构优化,提高小分子药物筛选优化效率,从而设计出具有良好生物学活性和临床开发潜力的候选化合物分子。
通过这种方式,首药控股提高了候选化合物分子的筛选效率和成功率,使得其拥有大量的候选药物和创新药研发管线。优质临床前候选药物的确立,保障了临床试验的稳步推进,使得新药研发周期有效缩短。
其次是在研发成本上,首药控股的控制成本能力相当出众。招股书显示,首药控股11款自研产品三年半以来的研发费用合计仅2.14亿元,整体预算投入仅为21.3亿元,平均每款创新药研发费用仅需不到2亿元!
此外,在商业化策略上,首药控股已经在北京经济开发区筹建研发及产业化基地,为后续新药上市后的大规模生产提供充足的产能保证。同时准备自建营销团队,开展市场教育、建立销售网络,并不惧同类产品竞争,将争取尽快纳入国家医保目录作为销售的重要手段,以促进产品全面推广。
以首药控股在新药研发上的效率和低成本,未来在医保谈判或集采中,与其他相同靶点创新药比在成本上将更有优势。或许在不久的将来,中国患者真的能够通过医保,以较低的医保后价格吃到首药控股的创新肿瘤药。
解决科研工作者的后顾之忧
与许多创新药企不同的是,首药控股的创始人李文军不是生物医药科班出身,在未从事生物医药行业之前,他曾在体制内、外摸爬滚打多年。
或许正是这种不同的经历,让首药控股的企业文化显得与众不同。在对待研发人才方面,李文军为研发人员创造了宽松的研发环境,赋予核心研发团队极大的研发决策权,发挥研发人员的主人翁精神。
由于公司地处首都北京,首药控股为让研发人员专注、专心从事创新药研发,不被外界因素困扰,积极为研发人员争取各项人才福利政策和科技荣誉。
此外,为激励公司员工的积极性,公司设立以研发人员为主的员工持股平台。2020年首药控股开展了大规模的员工持股计划,最终确认股份支付费用高达2.43亿元,员工持股人数比例超过50%。
截至2021年6月末,首药控股共有员工142人,其中研发人员122人,研发人员占员工总数的比例高达85.92%。
通过股权激励,员工可分享公司发展所带来的股权增值收益,留住人才的同时,进一步保证员工的研发热情和积极性,为持续创新赋能。
为进一步吸引及选拔优秀人才,首药控股计划在未来持续推出对核心员工股权激励、提升员工薪酬福利水平,以不断吸引和留住优秀研发人才。
结语
中国创新药既需要创造力、前瞻性,也需要有情怀、有社会责任感。首药控股手握23个创新药研发管线,在获得上市融资后,资金实力将得到明显增强,在研产品临床进度及新产品研究将得到更有效的支持,如何兑现其“造中国患者能够吃得起的一类新药”目标值得期待。(贝壳社 陈正青)
参考资料
1.首药控股招股书,官网
2.《里程碑,北京本土孵化投资!首药控股科创板过会》,药融圈,2021.8.3
3.《外行“搞出”抗癌创新药——首药控股董事长李文军》,光明网,2020.1.2
